Молниеносная пурпура
Молниеносная пурпура (МП) развивается у новорождённых с врождённым дефицитом протеинов С или S, больных, перенёсших тяжёлые инфекционные заболевания, и пациентов с бактериальным сепсисом. Гомозиготное носительство дефектных генов, кодирующих продукцию протеинов С или S, приводит к впутрисосудистому тромбообразованию, что клинически выражается в виде МП. Постинфекционная форма заболевания обычно развивается через 7-10 дней после инфицирования.
МП может быть осложнением ветряной оспы, скарлатины, вирусной экзантемы и реакций гиперчувствительности. Постинфекционная МП обычно протекает относительно мягко, без поражения внутренних органов. Показано, что в некоторых случаях её развитие связано с образованием в крови пациента антител против протеина S. Третий вариант МП развивается при сепсисах вследствие инфицирования бактериями, продуцирующими эндотоксины, В большинстве случаев возбудителем служит Neisseria meningitidis, реже — Streptococcus pneumoniae, стрептококки группы А и В, Haemophilis nfluenza и Capnocytophaga canimosus (штамм DF-2, проникающий в кровь при укусах собак). Особенно предрасположены к этой форме МП лица с врождённым повышением свёртываемости крови в результате мутации в гене, кодирующем продукцию фактора свёртывания крови V (Лейден).
Развитие молниеносной пурпуры отражает наличие патологии, которая может быть вызвана рядом причин. Причиной диссеминированного внутрисосудистого свёртывания крови считают выраженную коагулопатию. При сепсисе бактериальный эндотоксин и комплемент атакуют эндотелий кровеносных сосудов и нарушают его целостность. В результате тканевый фактор свёртывания крови проникает в кровь и образует комплекс с фактором свёртывания VII, который, в свою очередь, активирует фактор V, X, VIII и IX. Конечный результат этой цепи событий — активация тромбина и других белков-медиаторов свёртывания крови. Протеин С — зависимый от витамина К гликопротеид, в норме циркулирующий в крови в неактивной форме. При активации системы свёртывания тромбин связывается с тромбомодулином, экспрессирующимся на мембранах эндотелиоцитов. Неактивный протеин С способен к взаимодействию с комплексом «тромбин-тромбомодулин» и связыванию со специальным рецептором, присутствующим на клетках эндотелия, в результате чего происходит его активация. Активированный протеин С и его кофактор (протеин S) связываются с факторами свёртывания V и VIII в крови, инактивируя их. В результате свёртываемость крови уменьшается.
Не исключено, что именно нарушения в системе активации протеина С приводят к развитию МП при менингококковом сепсисе. В пользу этого предположения свидетельствует тот факт, что при сепсисе, осложнившемся МП, активный протеин С в крови больных практически отсутствует (его концентрация ниже определяемой). При этом введение неактивного протеина С извне не изменяет ситуацию. Более того, доказано, что в эндотелиоцитах у таких больных, как правило, снижены экспрессия тромбомодулина и количество рецепторов к протеину С, что приводит к уменьшению вероятность активации протеина С. Такое нарушение равновесия в системе свёртывания крови неизбежно вызывает увеличение вероятности случайного тромбообразования.
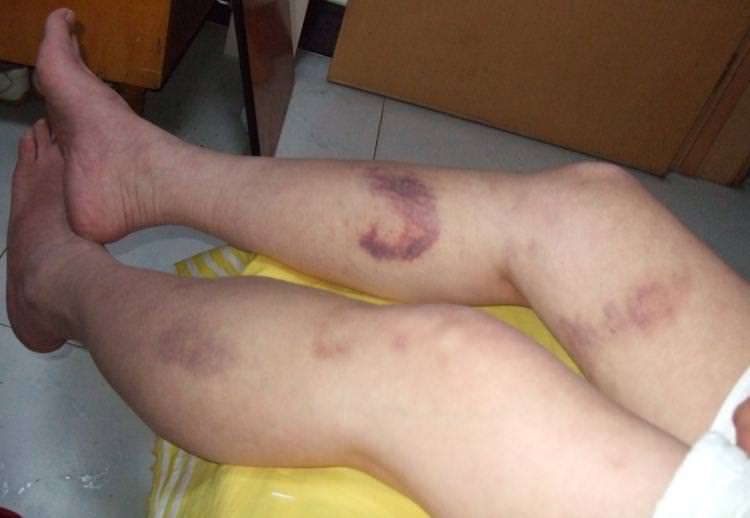
Клинически МП манифестирует внезапным образованием увеличивающихся болезненных пурпурозных папул и бляшек, окружённых эритематозным кольцом. В дальнейшем в центре этих элементов возникает некротическая зона, формирование которой иногда сопровождается образованием везикул или пузырей, а затем струпа. Чаще всего поражаются дистальные участки конечностей. При постинфекционнэй форме МП возможно поражение всей конечности. Как правило, подобные очаги формируются и во внутренних органах. Для возникновения МП необходимо развитие синдрома диссеминированного внурисосудистого свёртывания крови. Это обстоятельство позволяет дифференцировать МП с кожными некротическими очагами, образующимися под действием гепарина или кума див a тромботической тромбэцитопенической пурпурой, криоглобулинемией и состоянием, характеризующимся присутствием в крови антител против фосфолипидов. При МП в крови больного обычно снижено содержание фибриногена, факторов V и VIII, протеинов С к S, антитромбина III и количество тромбоцитов. При этом увеличивается прстромбиновое и парциальное тромбопластиновое время, повышено содержание продуктов распада фибрина, в частности D-димеров. При гистологическом исследовании биоптатов кожи обнаруживают тромбоз сосудов, отложения фибрина, тромбоцитар- ные агрегаты и лейкоцитарную инфильтрацию. Если причиной МП послужила менингококкемия, то иногда обнаруживают грамотрицательные диплококки. При МП, связанной с бактериальным сепсисом, нейтрофильный васкулит может сопровождаться тромбозом, что отличает его от заболевания, не связанного с инфекцией.
Лечение молниеносной пурпуры
Лечение МП должно быть направлено на устранение причины возникновения заболевания и предотвращение синдрома диссеминированного внутрисосудистого свёртызания крови. На этапе лечения рекомендована консультация хирурга. Необходимы контроль над состоянием пациента, своевременная диагностика осложнений, например тяжёлых туннельных синдромов (особенно на фоне агрессивной инфузионной терапии). Туннель — ограниченная фасциями анатомическая зона, в которой в условиях отёка и недостаточного кровоснабжения часто развиваю некротические очаги. При образовании туннельного синдрома рекомендовано срочное проведение хирургического вмешательства (рассечение фасций и дренирование туннеля). В некоторых случаях постинфекционная МП возникает вследствие образования антител против протеина S. У таких больных хороший терапевтический эффект приносят плазмаферез или введение иммуноглобулинов в дополнение к другим лечебным мероприятиям.
Лечение менингококкемии начинают немедленно после подтверждения диагноза данными бактериологического исследования. Время начала терапии напрямую с прогнозом заболевания. До подтверждения диагноза и определения типа антибактериального средства применяют внутривенные инъекции цефалоспоринов третьего поколения. При необходимости проводят инфузионную терапию, вводят инотропные препараты. Если у пациента развивается МП. сопровождающаяся обширным поражением кожи, то прогноз, как правило, неблагоприятный. Доказано, что выраженный терапевтический эффект при сепсисе приносит введение активированного протеина С и бактерицидные белков, увеличивающих проницаемость мембран (связывают бактериальные эндотоксины и обрывают каскад событий, приводящих к генерализованному воспалению). По данным некоторых исследований, эффективным считают применение антител против бактериального эндотоксина, ФНО-ос и ИЛ-lp, системных глюкокортикоидов, негктивированного протеина С, свежезамороженной донорской плазмы, антитромбина III, гепарина, тканевого активатора плазминогена, а также проведение и экстракорпоральной мембранной оксигенации. Назначение ан гикоагулянтов может осложниться кровотечением, поэтому при их использовании требуется соблюдать особую осторожность.
Неблагоприятные признаки, ухудшающие прогноз менингококкемии: образовавшиеся на коже менее чем за 12 ч до госпитализации больного; гипотензия (систгшческое артериальное давление менее 70 мм рт-с.): отсутствие симптомов менингита; количество лейкоцитов в периферической крови менее 10×10/# СОЭ менее 10 мм/ч; разница между ректальной температурой и температурой тела более 3 °С; ухудшение состояния больного в течение последнего часа. Смертность при менкнюкоккемии составляет S -10%.
Отдаленные последствия менингококкемии связаны с ишемическим повреждением тканей в острой фазе заболевания, В некоторых случаях может потребоваться ампутация конечностей, возможно нарушение нормального роста костей. Пациентам, перенёсшим острую фазу заболевания, рекомендовано обследование. позволяющее оценить состояние системы комплемента и определить титр антител в крови. На основании его результатов принимают решение о необходимости проведения соответствующей заместительной терапии.
В целях предупреждения эпидемического распространения менингококковой инфекции обязательный курс профилактической терапии должны пройти все лица, контактировавшие с больным мениш ококкемией. Мснингококковая вакцина состоит из четырёх основных компонентов (очищенных полисахаридов бактериальных капсул типа А. С, Y и W-135). Полисахарид типа В из состава вакцины исключён, поскольку он вызывает слабый иммунный ответ. Мепингококковую вакцину применяют для активной иммунизации военнослужащих и профилактики возникновения эпидемий. Кроме того, её введение рекомендовано лицам, имеющим наследственных или приобретенные дефекты в системе комплемента, а также пациентам после спленктсмии.





























Leave a Response