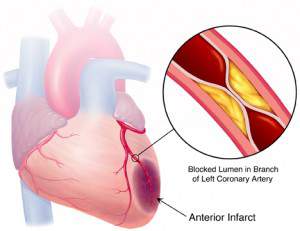
Коронарные сосуды
Атеросклероз — наиболее распространенный патологический процесс, поражающий коронарные и периферические артерии у взрослого человека. Этот процесс лежит в основе преобладающего влияния сосудистых заболеваний как причины смертности в современном обществе. Подходы к лечению этого заболевания включают модификацию факторов риска, использование фармакологических препаратов и процедуры реваскуляризации.
Подгруппа пациентов, которые не отвечают требованиям выполнения процедур реваскуляризации, продолжает испытывать клинические проявления ишемии миокарда или конечностей, несмотря на оптимальную медикаментозную терапию. Эта патофизиология рефрактерной и не подлежащей реваскуляризации ишемии ткани стала мишенью стратегии генной терапии, имеющей генерическое название «терапевтический ангиогенез». Еще в одной группе пациентов развиваются рецидивирующие симптомы после реваскуляризации, обусловленные ремоделированием сосуда после вмешательства.
Такое ремоделирование приводит к рестенозу целевой артерии или обходного шунта. Высокая частота рестеноза после вмешательства и неудовлетворительные варианты лечения привели к разработке нескольких подходов, основанных на генной терапии и нацеленных на этот патофизиологический процесс. Дополнительной целью для переноса генов стал процесс тромбоза, который не только способствует патогенезу атеросклероза, но также обусловливает многие осложняющие течение заболевания острые клинические синдромы. В следующем разделе мы будем обсуждать модели генной терапии с целью вызвать терапевтический ангиогенез, антирестеноз и антитромбоз.
Терапевтический ангиогенез стал наиболее частым вмешательством среди большого количества появляющихся необщепринятых стратегий реваскуляризации. Причины такой заметной роли ангиогенеза: эффективность ангиогенных цитокинов для индуцирования формирования новых сосудов, использование простой технологии переноса гена для достижения эффекта, низкий порог для осуществления фенотипического эффекта и наличие методик, облегчающих доставку вектора в клинических условиях.
Ангиогенез и последующее ослабление ишемии мышцы были продемонстрированы при переносе гена, опосредованном через плазмиды и аденовирусный вектор. Для коррекции этого патофизиологического процесса достаточно вызвать транзиторный тип экспрессии гена. Было сообщено о подобных исходах, когда использовались интегрирующие векторы, такие как рААВ. Однако если в этом контексте наблюдается стабильная и продолжительная трансгенная экспрессия, то могут возникать нежелательные эффекты. Одно из потенциальных решений этой проблемы, сохраняющих преимущества интегрирующего вектора, — создание отвечающего на гипоксию промотерного элемента в экспрессионной кассете.
Применение терапевтического ангиогенеза при заболевании периферических артерий начало развиваться раньше, чем использование этой технологии при ИБС. Хотя генные методы свидетельствуют о существенном прогрессе в лечении критической ишемии конечности вследствие ЗПА, это заболевание также представляет собой модель сосудистой недостаточности в конечной стадии. Она очень хорошо подходит для вмешательств, основанных на генной терапии, и для объективной оценки терапевтических конечных точек. Потенциально успешные вмешательства на периферии можно экстраполировать на лечение рефрактерной ишемии миокарда. Доклинические исследования и клинические исследования ранней фазы стабильно давали положительные результаты после внутриартериальной или внутримышечной, опосредованной через плазмиды, доставки рекомбинантных ангиогенных цитокинов в контексте ЗПА.
Однако в недавних исследованиях II фазы представлена объективная оценка клинического улучшения у пациентов с ЗПА, леченных аденовирусным вектором, кодирующим сосудистый эндотелиальный фактор роста, либо VEGF165 в аденовирусном или липосомальном векторе. Данное улучшение не превышало такового в группе плацебо. Однако было выявлено улучшение васкуляризации, степень которой оценивали ангиографически. Полученные результаты подчеркивают важность соответствующего контроля при оценке эффективности новых терапевтических вмешательств. Множество параметров могут варьировать при изменении дизайна исследований такого типа. На исход исследования влияют такие переменные, как подбор и количество пациентов, измеряемые конечные точки, выбор ангиогенного фактора или комбинации факторов, доза и тип вектора, а также метод его доставки. Несомненно, в дизайн будущих исследований войдут такие переменные.
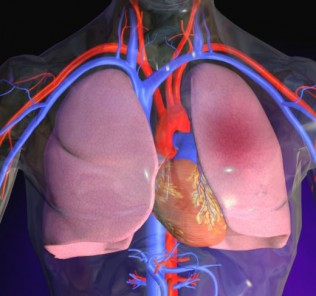
Доктором Jeffrey Isner было начато первое клиническое исследование терапевтического ангиогенеза при ишемии миокарда. Пациенты с рефрактерными симптомами получали лечение плазмидами, кодирующими VEGF165 с помощью непосредственной инъекции через мини-торакотомический разрез. В этой группе пациентов наблюдали улучшение симптомов и миокардиальной перфузии, доказанное с помощью радиоизотопного сканирования перфузии и электромеханических карт. Впоследствии сообщали об успешном проведении терапевтического ангиогенеза.
У данных пациентов его достигли в исследованиях ранней фазы с использованием трансэндокардиального подхода, основанного на применении катетеров. Сначала идентифицировали ишемический миокард, а после этого определяли анатомическое положение кончика катетера с помощью системы электромеханического картирования. Сообщали, что у пациентов, получавших VEGF165 при таком подходе, достигали как субъективного, так и объективного улучшения, по сравнению с инъекциями плацебо.




























Leave a Response