Заболевание характеризуется аутосомно-рецессивным типом наследования
К пониманию патогенеза синдрома Луи-Бар ведет выявление у больных спонтанных хромосомных разрывов, перестроек 7-й и 14-й хромосом, транслокации 14:14. Специальными исследованиями установлены нестабильность генома и нарушения механизмов репарации ДНК, характерные для данного синдрома. В части случаев вилочковая железа сохраняла архитектонику эмбрионального типа.
Прогноз синдрома неблагоприятен. Около половины летальных исходов обусловлено хроническими поражениями бронхолегочной системы, около 20% связано с развитием злокачественных процессов, остальные случаи — с сочетанием этих причин; некоторые больные доживают до 40-50 лет.
ИДС с гипер-IgM характеризуется сниженным содержанием IgA и IgG, нормальным или повышенным уровнем IgM в плазме крови. Содержание IgM колеблется от 1,5 до 10 мг/мл, т. е. от 1,5 до 10 г/л. Кроме повышенной чувствительности к инфекции, у больных наблюдается образование аутоантител к гранулоцитам, тромбоцитам, что проявляется тромбоцитопенией, нейтропенией, склонностью к аутоиммунным заболеваниям почек и крови. Этот вид дисгаммаглобулинемии наследуется по рецессивному типу, связан с полом. При гистологическом исследовании биоптатов лимфатических узлов обнаруживаются сформированные фолликулы, а также плазмоциты. При люминесцентной микроскопии отмечается яркая флюоресценция клеток после воздействия анти-М — сывороткой, меченной флюоресцеином.
Более тяжелые формы заболевания отмечаются при сочетании данного типа гипогаммаглобулинемии с гранулоцитопенией, но она наблюдается непостоянно. Содержание лимфоцитов и плазмоцитов в крови повышено, однако лимфатические узлы не имеют зародышевых центров. Вилочковая железа может быть гиперплазирована, но структура ее нормальна. В костном мозге обнаруживается задержка созревания миелоидных элементов, которые отличаются низкой фагоцитарной активностью. Установлен аутосомно-рецессивный тип наследования этого иммунодефицитного состояния.
Известно, что при гипер-М-синдроме отмечается низкая активность Т-лимфоцитов-хелперов. Считается, что лимфоциты больных имеют сходство с Т — и В-лимфоцитами новорожденных, т. е. в основе может лежать нарушение переключения синтеза иммуноглобулинов на «взрослый» тип.
Исследования, проведенные у больных с Х-сцепленной гипогаммаглобулинемией при нормальном или повышенном содержании IgM в крови, показали, что в этом случае ген постоянного участка тяжелой цепи IgM не подвергается делеции. Это блокирует переключение синтеза иммуноглобулинов, так как гены CY и Са не подвергаются перегруппировке. При этом имеет место раннее ограничение транскрипции, заканчивающееся на уровне гена тяжелой цепи IgM. Другой механизм развития ИДС с гипер-IgM обусловлен мутацией регуляторных генов Х-хромосомы. Е. J. Mensink и соавт. установили положение локуса ИДС с гипер-IgM на Х-хромосоме Xq — q27. Этот локус обозначен символом ХНМ и отличен от локуса Х-сцепленной агаммаглобулинемии.
Гипер-IgD с периодической лихорадкой. J. W. Van der Меег и соавт. описали новый синдром, характеризующийся рецидивирующими лихорадочными состояниями, головными болями, увеличением миндалин, лейкоцитозом. Определенной периодичности этих явлений нет. Приступы удается предупредить препаратами колхицина. Плазматический уровень IgD повышен до 5300 МЕ/л при норме до 150. Тип наследования этого синдрома пока не установлен.
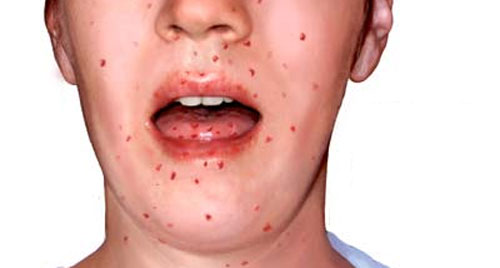
Гипер-Е-синдром. В 1966 г. С. D. Davis и соавт. описали синдром Джоба, получивший также название «гипер-IgE- синдрома», синдрома «золотистого стафилококка» с гипер-IgE, синдрома Hie. Заболевание проявляется в первые месяцы жизни пиодермией с генерализованным экзематозным дерматитом. Нередко больные отличаются грубыми чертами лица. Поражается кожа лица, волосистой части головы, шеи. Типичны повторные пневмонии, рецидивирующие отиты, синуситы, хронический ринит, конъюнктивит. В результате гнойных процессов образуются спайки, рубцы на коже. Под кожей нередки «холодные» абсцессы. Кожные процессы сопровождаются сильным зудом. Поражения легких проявляются в виде буллезной пневмонии. Однако перехода этого синдрома в сепсис не наблюдается, не бывает остеомиелитов, менингита. Несмотря на повышение содержания IgE в крови, проявления атопии отсутствуют, бронхиальная астма и атопический дерматит не развиваются. В крови эозинофилия, иногда весьма значительная. Ей сопутствует нейтрофилез со сдвигом влево. В структуре IgE находят антистафилококковые антитела в высоких титрах.
Отмечается сниженная продукция антител класса IgG на антигены стафилококка, недостаточность Т-супрессоров по отношению к BE клону лимфоцитов. Отмечено снижение хемотаксиса гранулоцитов. Возможно, он обусловлен избыточной продукцией гистамина под влиянием активации тучных клеток IgE. Другое объяснение — секреция мононуклеарными клетками фактора, подавляющего хемотаксис. Лейкоциты больных способны в избытке генерировать токсические радикалы кислорода, с чем связывается, в частности, формирование холодных абсцессов в подкожной клетчатке.
Синдром Джоба наследуется по аутосомно-рецессивному типу, но известны его варианты, наследующие аутосомно-доминантным путем.



























Leave a Response